Politetrafluoroetilen (politetrafluoroetilen) je vjerovatno najčešće korišteni fluoropolimer jer ima nekoliko karakteristika koje ga čine idealnim materijalom za širok spektar primjena. Fleksibilniji je od drugih sličnih cijevi i otporan je na gotovo sve industrijske hemikalije.
Temperaturni raspon je približno od -330°F do 500°F, što pruža najširi temperaturni raspon među fluoropolimerima. Osim toga, ima odlična električna svojstva i nisku magnetsku permeabilnost. Ptfe cijevi su najčešće korištene laboratorijske cijevi i primjene gdje su hemijska otpornost i čistoća bitni.PTFEima vrlo nizak koeficijent trenja i jedna je od najklizajućih poznatih supstanci
Karakteristike:
100% čista PTFE smola
U poređenju sa FEP, PFA, HP PFA, UHP PFA, ETFE, ECTFE, najfleksibilnijim fluoropolimernim cijevima
Hemijski inertan, otporan na gotovo sve industrijske hemikalije i rastvarače
Širok temperaturni raspon
Niska penetracija
Glatka neljepljiva površina
Najniži koeficijent trenja
Odlične električne performanse
Nezapaljivo
Netoksično
Primjene:
laboratorija
Hemijski proces
Oprema za analizu i procese
Praćenje emisija
Niska temperatura
visoka temperatura
Električna energija
ozon
Struktura molekula PTFE-a
Politetrafluoroetilen (PTFE) se proizvodi polimerizacijom mnogih molekula tetrafluoroetilena
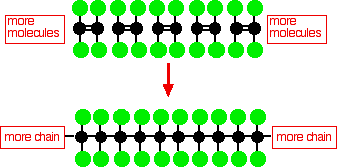
Ovaj jednostavni PTFE dijagram ne prikazuje trodimenzionalnu strukturu molekule. U jednostavnijem molekularnom poli(etilenu), ugljični lanac molekule povezan je samo atomima vodika, a ovaj lanac je vrlo fleksibilan - definitivno nije linearna molekula.
Međutim, u politetrafluoroetilenu, atom fluora u CF2 grupi je dovoljno velik da interferira s atomom fluora na susjednoj grupi. Morate imati na umu da svaki atom fluora ima 3 para slobodnih elektrona koji strše.
Efekat ovoga je suzbijanje rotacije jednostruke veze ugljik-ugljik. Atomi fluora imaju tendenciju da budu raspoređeni tako da budu što dalje od susjednih atoma fluora. Rotacija obično uključuje sudare usamljenih parova između atoma fluora na susjednim atomima ugljika, što rotaciju čini energetski nepovoljnom.
Odbojna sila zaključava molekulu u oblik štapića, a atomi fluora su raspoređeni u vrlo blagoj spirali - atomi fluora su raspoređeni u spiralu oko ugljikovog lanca. Ove olovne trake će biti stisnute zajedno poput dugih, tankih olovaka u kutiji.
Ovaj bliski kontaktni raspored ima važan utjecaj na intermolekularne sile, kao što ćete vidjeti
Međumolekularne sile i tačka topljenja PTFE-a
Tačka topljenja politetrafluoroetilena navodi se kao 327°C. Ovo je prilično visoko za ovaj polimer, tako da između molekula moraju postojati značajne van der Waalsove sile.
Zašto ljudi tvrde da su van der Waalsove sile u PTFE-u slabe?
Van der Waalsova disperziona sila uzrokovana je privremenim fluktuirajućim dipolima koji nastaju kada se elektroni u molekulu kreću. Budući da je molekula PTFE-a velika, očekivali biste veliku disperzionu silu jer postoji mnogo elektrona koji se mogu kretati.
Općenito, što je molekula veća, to je veća disperzijska moć.
Međutim, PTFE ima problem. Fluor je vrlo elektronegativan. On ima tendenciju da čvrsto veže elektrone u vezi ugljik-fluor, tako čvrsto da se elektroni ne mogu kretati kao što mislite. Vezu ugljik-fluor opisujemo kao vezu koja nema jaku polarizaciju.
Van der Waalsove sile također uključuju dipol-dipol interakcije. Ali u politetrafluoroetilenu (PTFE), svaki molekul je okružen slojem blago negativno nabijenih atoma fluora. U ovom slučaju, jedina moguća interakcija između molekula je međusobno odbijanje!
Dakle, sila disperzije je slabija nego što mislite, a dipol-dipol interakcija će uzrokovati odbijanje. Nije ni čudo što ljudi kažu da je van der Waalsova sila u PTFE-u vrlo slaba. Zapravo nećete dobiti silu odbijanja, jer je utjecaj sile disperzije veći od utjecaja dipol-dipol interakcije, ali neto učinak je da će van der Waalsova sila težiti slabljenju.
Ali PTFE ima vrlo visoku tačku topljenja, tako da sila koja drži molekule zajedno mora biti vrlo jaka.
Kako PTFE može imati visoku tačku topljenja?
PTFE je vrlo kristalan, u tom smislu postoji velika površina, molekule su u vrlo pravilnom rasporedu. Zapamtite, molekule PTFE-a se mogu smatrati izduženim štapićima. Ovi polovi će biti blisko grupirani zajedno.
To znači da iako molekula ptfe ne može proizvesti zaista velike privremene dipole, dipoli se mogu vrlo efikasno koristiti.
Dakle, jesu li van der Waalsove sile u PTFE-u slabe ili jake?
Mislim da oboje možete biti u pravu! Ako su lanci politetrafluoroetilena (PTFE) raspoređeni na takav način da nema prebliskog kontakta između lanaca, sila između njih će biti vrlo slaba, a tačka topljenja vrlo niska.
Ali u stvarnom svijetu, molekule su u bliskom kontaktu. Van der Waalsove sile možda nisu toliko snažne koliko bi mogle biti, ali struktura PTFE-a znači da osjećaju najveći učinak, stvarajući ukupno jake intermolekularne veze i visoke tačke topljenja.
To je u suprotnosti s drugim silama, poput sile interakcije dipol-dipol, koja se smanjuje samo 23 puta, ili dvostruka udaljenost se smanjuje 8 puta.
Stoga, čvrsto pakovanje molekula u obliku štapića u PTFE maksimizira efikasnost disperzije.
Neljepljiva svojstva
Zbog toga se voda i ulje ne lijepe za površinu PTFE-a i zato možete pržiti jaja u tavi obloženoj PTFE-om bez lijepljenja za tavu.
Morate uzeti u obzir koje sile mogu fiksirati druge molekule na površiniPTFEMože uključivati neku vrstu hemijske veze, van der Waalsovu silu ili vodoničnu vezu.
Hemijsko vezivanje
Veza ugljik-fluor je vrlo jaka i nemoguće je da bilo koji drugi molekul dođe do ugljikovog lanca kako bi izazvao bilo kakvu reakciju supstitucije. Nemoguće je da dođe do hemijske veze.
van der Waalsove sile
Vidjeli smo da van der Waalsova sila u PTFE-u nije jako jaka i da će PTFE imati visoku tačku topljenja samo zato što su molekule toliko blizu da imaju vrlo efikasan kontakt.
Ali drugačije je za druge molekule blizu površine PTFE-a. Relativno male molekule (kao što su molekule vode ili molekule ulja) imat će samo mali kontakt s površinom i generirat će se samo mala količina van der Waalsove privlačnosti.
Veliki molekul (kao što je protein) neće biti u obliku štapića, tako da nema dovoljno efikasnog kontakta između njega i površine da bi se prevazišla tendencija niske polarizacije PTFE-a.
U svakom slučaju, van der Waalsova sila između površine PTFE-a i okolnih stvari je mala i neefikasna.
Vodikove veze
Molekule PTFE-a na površini su potpuno obavijene atomima fluora. Ovi atomi fluora su vrlo elektronegativni, tako da svi nose određeni stepen negativnog naboja. Svaki atom fluora također ima 3 para izbočenih usamljenih elektrona.
Ovo su uslovi potrebni za formiranje vodoničnih veza, kao što su slobodni par na fluoru i atom vodonika u vodi. Ali to se očigledno neće dogoditi, inače će postojati jaka privlačnost između molekula PTFE i molekula vode, i voda će se zalijepiti za PTFE.
Sažetak
Ne postoji efikasan način da se drugi molekuli uspješno pričvrste na površinu PTFE-a, tako da on ima neljepljivu površinu.
Nisko trenje
Koeficijent trenja PTFE-a je vrlo nizak. To znači da ako imate površinu obloženu PTFE-om, druge stvari će lako kliziti po njoj.
U nastavku slijedi kratak sažetak onoga što se događa. Ovo je iz rada iz 1992. godine pod nazivom "Trenje i habanje politetrafluoroetilena".
Na početku klizanja, PTFE površina se lomi i masa se prenosi na mjesto gdje se klizi. To znači da će se PTFE površina istrošiti.
Kako se klizanje nastavilo, blokovi su se raspadali u tanke filmove.
Istovremeno, površina PTFE-a se izvlači kako bi se formirao organizovani sloj.
Obje površine u kontaktu sada imaju dobro organizirane PTFE molekule koje mogu kliziti jedna po drugoj
Gore navedeno je uvod u politetrafluoroetilen, politetrafluoroetilen se može preraditi u razne proizvode, specijalizirani smo za izradu PTFE cijevi.proizvođači PTFE crijeva, dobrodošli da komunicirate s nama
Pretrage povezane sa ptfe crijevom:
Vrijeme objave: 05.05.2021.





