Polytetrafluorethylen (polytetrafluorethylen) je pravděpodobně nejpoužívanějším fluoropolymerem, protože má několik vlastností, které z něj činí ideální materiál pro širokou škálu aplikací. Je pružnější než jiné podobné trubky a odolává téměř všem průmyslovým chemikáliím.
Teplotní rozsah je přibližně -330 °F až 500 °F, což poskytuje nejširší teplotní rozsah mezi fluoropolymery. Kromě toho má vynikající elektrické vlastnosti a nízkou magnetickou permeabilitu. PTFE trubky jsou nejrozšířenější laboratorní trubky a aplikace, kde je nezbytná chemická odolnost a čistota.PTFEmá velmi nízký koeficient tření a je jednou z nejkluznějších známých látek
Vlastnosti:
100% čistá PTFE pryskyřice
Ve srovnání s FEP, PFA, HP PFA, UHP PFA, ETFE, ECTFE, nejflexibilnějšími fluoropolymerovými trubkami
Chemicky inertní, odolný vůči téměř všem průmyslovým chemikáliím a rozpouštědlům
Široký teplotní rozsah
Nízká penetrace
Hladký nepřilnavý povrch
Nejnižší koeficient tření
Vynikající elektrický výkon
Nehořlavý
Netoxický
Aplikace:
laboratoř
Chemický proces
Analytické a procesní zařízení
Monitorování emisí
Nízká teplota
vysoká teplota
Elektřina
ozón
Struktura molekul PTFE
Polytetrafluorethylen (PTFE) se vyrábí polymerací mnoha molekul tetrafluorethylenu
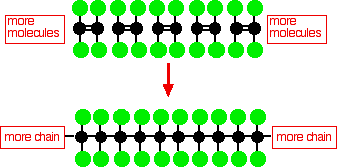
Tento jednoduchý PTFE diagram nezobrazuje trojrozměrnou strukturu molekuly. V jednodušší molekule poly(ethylenu) je uhlíkový řetězec molekuly propojen pouze atomy vodíku a tento řetězec je velmi flexibilní – rozhodně se nejedná o lineární molekulu.
V polytetrafluorethylenu je však atom fluoru ve skupině CF2 dostatečně velký, aby interferoval s atomem fluoru na sousední skupině. Je třeba si uvědomit, že každý atom fluoru má 3 páry volných elektronů.
Důsledkem je potlačení rotace jednoduché vazby uhlík-uhlík. Atomy fluoru mají tendenci být uspořádány tak, aby byly co nejdále od sousedních atomů fluoru. Rotace obvykle zahrnuje srážky volných párů mezi atomy fluoru na sousedních atomech uhlíku, což činí rotaci energeticky nevýhodnou.
Odpudivá síla uzamkne molekulu do tvaru tyčinky a atomy fluoru jsou uspořádány ve velmi jemné spirále – atomy fluoru jsou uspořádány ve spirále kolem uhlíkového řetězce. Tyto olověné proužky budou stlačeny k sobě jako dlouhé, tenké tužky v krabičce.
Jak uvidíte, toto těsné kontaktní uspořádání má důležitý vliv na mezimolekulární síly.
Mezimolekulární síly a bod tání PTFE
Teplota tání polytetrafluorethylenu je uváděna na 327 °C. To je pro tento polymer poměrně vysoká hodnota, takže mezi molekulami musí existovat značné van der Waalsovy síly.
Proč lidé tvrdí, že van der Waalsovy síly v PTFE jsou slabé?
Van der Waalsova disperzní síla je způsobena dočasnými kolísavými dipóly, které vznikají při pohybu elektronů v molekule. Vzhledem k tomu, že molekula PTFE je velká, dalo by se očekávat velkou disperzní sílu, protože se může pohybovat mnoho elektronů.
Obecně platí, že čím větší je molekula, tím větší je disperzní schopnost.
PTFE má však jeden problém. Fluor je velmi elektronegativní. Má tendenci vázat elektrony ve vazbě uhlík-fluor pevně k sobě, tak pevně, že se elektrony nemohou pohybovat, jak si myslíte. Vazbu uhlík-fluor popisujeme jako nesilně polarizovanou.
Van der Waalsovy síly zahrnují i dipól-dipólové interakce. Ale v polytetrafluorethylenu (PTFE) je každá molekula obklopena vrstvou mírně záporně nabitých atomů fluoru. V tomto případě je jedinou možnou interakcí mezi molekulami vzájemné odpuzování!
Disperzní síla je tedy slabší, než si myslíte, a dipól-dipólová interakce způsobí odpudivé síly. Není divu, že se říká, že van der Waalsova síla v PTFE je velmi slabá. Ve skutečnosti odpudivou sílu nepocítíte, protože vliv disperzní síly je větší než vliv dipól-dipólové interakce, ale konečný výsledek je takový, že van der Waalsova síla bude mít tendenci slábnout.
Ale PTFE má velmi vysoký bod tání, takže síla, která drží molekuly pohromadě, musí být velmi silná.
Jak může mít PTFE vysoký bod tání?
PTFE je velmi krystalický, v tomto smyslu má velkou plochu a molekuly jsou uspořádány velmi pravidelně. Molekuly PTFE si lze představit jako protáhlé tyčinky. Tyto póly budou těsně seskupeny.
To znamená, že ačkoli molekula ptfe nemůže produkovat skutečně velké dočasné dipóly, lze tyto dipóly velmi efektivně využít.
Jsou tedy van der Waalsovy síly v PTFE slabé nebo silné?
Myslím, že můžete mít pravdu oba! Pokud jsou řetězce polytetrafluorethylenu (PTFE) uspořádány tak, že mezi nimi není příliš těsný kontakt, bude síla mezi nimi velmi slabá a bod tání bude velmi nízký.
Ale v reálném světě jsou molekuly v těsném kontaktu. Van der Waalsovy síly sice nemusí být tak silné, jak by mohly být, ale struktura PTFE znamená, že pociťují největší účinek, což vede k celkově silným mezimolekulárním vazbám a vysokým bodům tání.
To je v kontrastu s jinými silami, jako je například interakční síla dipól-dipól, která se zmenší pouze 23krát, neboli dvojnásobná vzdálenost se zmenší 8krát.
Pevné uspořádání tyčovitých molekul v PTFE proto maximalizuje účinnost disperze.
Nepřilnavé vlastnosti
Proto se voda a olej nelepí na povrch PTFE a proto můžete smažit vejce na pánvi s PTFE povlakem, aniž by se k pánvi přilepila.
Musíte zvážit, jaké síly by mohly fixovat další molekuly na povrchuPTFEMůže zahrnovat nějaký druh chemické vazby, van der Waalsovy síly nebo vodíkové vazby.
Chemická vazba
Vazba uhlík-fluor je velmi silná a je nemožné, aby se k uhlíkovému řetězci dostaly jakékoli jiné molekuly, které by způsobily jakoukoli substituční reakci. Je nemožné, aby došlo k chemické vazbě.
van der Waalsovy síly
Viděli jsme, že van der Waalsova síla v PTFE není příliš silná a způsobí, že PTFE bude mít pouze vysoký bod tání, protože molekuly jsou si tak blízko, že mají velmi efektivní kontakt.
U jiných molekul blízko povrchu PTFE je to ale jiné. Relativně malé molekuly (jako jsou molekuly vody nebo molekuly oleje) budou mít s povrchem jen malý kontakt a bude generováno jen malé množství van der Waalsovy přitažlivosti.
Velká molekula (například protein) nebude mít tyčinkovitý tvar, takže mezi ní a povrchem není dostatečně účinný kontakt, aby se překonala nízká polarizační tendence PTFE.
V obou případech je van der Waalsova síla mezi povrchem PTFE a okolními věcmi malá a neúčinná.
Vodíkové vazby
Molekuly PTFE na povrchu jsou zcela obaleny atomy fluoru. Tyto atomy fluoru jsou velmi elektronegativní, takže všechny nesou určitý stupeň záporného náboje. Každý atom fluoru má také 3 páry vyčnívajících volných elektronů.
Toto jsou podmínky nutné pro vznik vodíkových vazeb, jako je například volný pár na fluoru a atom vodíku ve vodě. To se ale samozřejmě nestane, jinak by mezi molekulami PTFE a molekulami vody existovala silná přitažlivost a voda by se k PTFE přilepila.
Shrnutí
Neexistuje žádný účinný způsob, jak by se jiné molekuly mohly úspěšně přichytit k povrchu PTFE, takže má nepřilnavý povrch.
Nízké tření
Koeficient tření PTFE je velmi nízký. To znamená, že pokud máte povrch potažený PTFE, ostatní věci na něm snadno uklouznou.
Níže je uveden stručný přehled toho, co se děje. Pochází z článku z roku 1992 s názvem „Tření a opotřebení polytetrafluorethylenu“.
Na začátku kluzu se povrch PTFE rozbije a hmota se přenese tam, kde se kluzná hmota pohybuje. To znamená, že se povrch PTFE opotřebuje.
Jak klouzání pokračovalo, bloky se rozvinuly do tenkých filmů.
Současně se povrch PTFE vytáhne a vytvoří organizovanou vrstvu.
Oba kontaktní povrchy nyní mají dobře organizované molekuly PTFE, které po sobě mohou klouzat.
Výše uvedené je úvod do polytetrafluorethylenu, polytetrafluorethylen lze vyrábět do různých produktů, specializujeme se na výrobu PTFE trubek.výrobci PTFE hadic, vítejte v komunikaci s námi
Vyhledávání související s PTFE hadicí:
Čas zveřejnění: 5. května 2021





