O politetrafluoroetileno (politetrafluoroetileno) é probablemente o fluoropolímero máis empregado porque ten varias características que o converten nun material ideal para unha ampla gama de aplicacións. É máis flexible que outras tubaxes similares e pode resistir case todos os produtos químicos industriais.
O rango de temperatura é de aproximadamente -160 °C a 260 °C, o que proporciona o rango de temperatura máis amplo entre os fluoropolímeros. Ademais, ten excelentes propiedades eléctricas e baixa permeabilidade magnética. Os tubos de PTFE son os tubos de laboratorio e as aplicacións máis empregadas onde a resistencia química e a pureza son esenciais.PTFEten un coeficiente de fricción moi baixo e é unha das substancias máis "escorregadizas" coñecidas
Características:
Resina de PTFE 100 % pura
En comparación con FEP, PFA, HP PFA, UHP PFA, ETFE, ECTFE, a maioría das tubaxes de fluoropolímero flexibles
Quimicamente inerte, resistente a case todos os produtos químicos e solventes industriais
Ampla gama de temperaturas
baixa penetración
Acabado superficial liso e antiadherente
Coeficiente de fricción máis baixo
Excelente rendemento eléctrico
Non inflamable
Non tóxico
Aplicacións:
laboratorio
proceso químico
Equipos de análise e proceso
Monitorización de emisións
Baixa temperatura
alta temperatura
electricidade
ozono
A estrutura das moléculas de PTFE
O politetrafluoroetileno (PTFE) fabrícase mediante a polimerización de moitas moléculas de tetrafluoroetileno
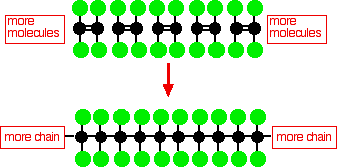
Este diagrama sinxelo de PTFE non mostra a estrutura tridimensional da molécula. No poli(etileno) molecular máis simple, a estrutura de carbono da molécula está conectada só por átomos de hidróxeno, e esta cadea é moi flexible; definitivamente non é unha molécula lineal.
Non obstante, no politetrafluoroetileno, o átomo de flúor nun grupo CF2 é o suficientemente grande como para interferir co átomo de flúor do grupo adxacente. Debes lembrar que cada átomo de flúor ten 3 pares de electróns solitarios que sobresaen.
O efecto disto é suprimir a rotación do enlace simple carbono-carbono. Os átomos de flúor tenden a estar dispostos o máis lonxe posible dos átomos de flúor adxacentes. A rotación tende a implicar colisións de pares solitarios entre átomos de flúor en átomos de carbono adxacentes, o que fai que a rotación sexa enerxeticamente desfavorable.
A forza repulsiva atrapa a molécula nunha forma de vara, e os átomos de flúor están dispostos nunha espiral moi suave: os átomos de flúor están dispostos en espiral arredor da cadea principal de carbono. Estas tiras de chumbo estarán apertadas como lapis longos e finos nunha caixa.
Esta disposición de contacto próximo ten unha influencia importante nas forzas intermoleculares, como veredes
Forzas intermoleculares e punto de fusión do PTFE
O punto de fusión do politetrafluoroetileno cítase como 327 °C. Isto é bastante alto para este polímero, polo que debe haber forzas de van der Waals considerables entre as moléculas.
Por que se afirma que as forzas de van der Waals no PTFE son débiles?
A forza de dispersión de van der Waals está causada polos dipolos fluctuantes temporais xerados cando os electróns da molécula se moven. Debido a que a molécula de PTFE é grande, esperaríase unha gran forza de dispersión porque hai moitos electróns que se poden mover.
A situación xeral é que canto maior sexa a molécula, maior será o poder de dispersión
Non obstante, o PTFE ten un problema. O flúor é moi electronegativo. Tende a unir os electróns da unión carbono-flúor con tanta forza que os electróns non se poden mover como se pensa. Describimos a unión carbono-flúor como algo que non ten unha polarización forte.
As forzas de van der Waals tamén inclúen interaccións dipolo-dipolo. Pero no politetrafluoroetileno (PTFE), cada molécula está rodeada por unha capa de átomos de flúor lixeiramente cargados negativamente. Neste caso, a única interacción posible entre as moléculas é a repulsión mutua!
Entón, a forza de dispersión é máis débil do que se pensa, e a interacción dipolo-dipolo causará repulsión. Non é de estrañar que a xente diga que a forza de van der Waals no PTFE é moi débil. En realidade, non se obtén a forza repulsiva, porque a influencia da forza de dispersión é maior que a da interacción dipolo-dipolo, pero o efecto neto é que a forza de van der Waals tenderá a debilitarse.
Pero o PTFE ten un punto de fusión moi alto, polo que a forza que mantén unidas as moléculas debe ser moi forte.
Como pode o PTFE ter un punto de fusión alto?
O PTFE é moi cristalino, neste sentido ten unha gran área e as moléculas están nunha disposición moi regular. Lembre que as moléculas de PTFE poden considerarse como varas alongadas. Estes polos estarán moi agrupados.
Isto significa que, aínda que a molécula de ptfe non pode producir dipolos temporais realmente grandes, os dipolos pódense usar de forma moi eficiente.
Entón, as forzas de van der Waals no PTFE son débiles ou fortes?
Creo que ambas as dúas poden ter razón! Se as cadeas de politetrafluoroetileno (PTFE) están dispostas de tal xeito que non haxa un contacto demasiado próximo entre elas, a forza entre elas será moi débil e o punto de fusión será moi baixo.
Pero no mundo real, as moléculas están en estreito contacto. Pode que as forzas de van der Waals non sexan tan potentes como poderían ser, pero a estrutura do PTFE fai que sexan as que senten o maior efecto, producindo enlaces intermoleculares fortes en xeral e puntos de fusión elevados.
Isto contrasta con outras forzas, como a forza de interacción dipolo-dipolo, que só se reduce 23 veces, ou o dobre de distancia, que se reduce 8 veces.
Polo tanto, o empaquetamento axustado de moléculas en forma de vara no PTFE maximiza a eficacia da dispersión.
As propiedades antiadherentes
Esta é a razón pola que a auga e o aceite non se pegan á superficie do PTFE e por que se poden fritir ovos nunha tixola revestida de PTFE sen que se peguen á tixola.
Debes considerar que forzas poderían fixar outras moléculas na superficie dePTFEPode incluír algún tipo de enlace químico, forza de van der Waals ou enlace de hidróxeno.
Enlaces químicos
A unión carbono-flúor é moi forte e é imposible que outras moléculas alcancen a cadea de carbono para provocar calquera reacción de substitución. É imposible que se produza unha unión química.
forzas de van der Waals
Vimos que a forza de van der Waals no PTFE non é moi forte e só fará que o PTFE teña un punto de fusión alto, porque as moléculas están tan próximas que teñen un contacto moi efectivo.
Pero é diferente para outras moléculas próximas á superficie do PTFE. As moléculas relativamente pequenas (como as moléculas de auga ou as moléculas de aceite) só terán un pequeno contacto coa superficie e só se xerará unha pequena cantidade de atracción de van der Waals.
Unha molécula grande (como unha proteína) non terá forma de vara, polo que non haberá suficiente contacto efectivo entre ela e a superficie para superar a baixa tendencia á polarización do PTFE.
De calquera xeito, a forza de van der Waals entre a superficie do PTFE e os obxectos circundantes é pequena e ineficaz.
Enlaces de hidróxeno
As moléculas de PTFE na superficie están completamente envoltas por átomos de flúor. Estes átomos de flúor son moi electronegativos, polo que todos levan un certo grao de carga negativa. Cada flúor tamén ten 3 pares de electróns solitarios sobresaíntes.
Estas son as condicións necesarias para a formación de enlaces de hidróxeno, como o par solitario no flúor e o átomo de hidróxeno na auga. Pero isto obviamente non ocorrerá, se non, haberá unha forte atracción entre as moléculas de PTFE e as moléculas de auga, e a auga adherirase ao PTFE.
Resumo
Non hai un xeito eficaz de que outras moléculas se unan á superficie do PTFE, polo que ten unha superficie antiadherente.
A baixa fricción
O coeficiente de fricción do PTFE é moi baixo. Isto significa que se tes unha superficie revestida con PTFE, outras cousas esvararán facilmente sobre ela.
A continuación móstrase un breve resumo do que está a suceder. Isto provén dun artigo de 1992 titulado "Fricción e desgaste do politetrafluoroetileno".
Ao comezo do deslizamento, a superficie de PTFE rómpese e a masa transfírese a onde se estea deslizando. Isto significa que a superficie de PTFE desgastarase.
A medida que o deslizamento continuaba, os bloques despregábanse en películas delgadas.
Ao mesmo tempo, a superficie do PTFE é estirada para formar unha capa organizada.
Ambas as superficies en contacto agora teñen moléculas de PTFE ben organizadas que poden deslizarse unha sobre a outra
O anterior é a introdución do politetrafluoroetileno. O politetrafluoroetileno pódese fabricar nunha variedade de produtos. Estamos especializados na fabricación de tubos de PTFE.fabricantes de mangueiras de PTFE, benvido a comunicarse con nós
Buscas relacionadas coa mangueira de PTFE:
Data de publicación: 05 de maio de 2021





