Polytetrafluóretylén (polytetrafluóretylén) je pravdepodobne najpoužívanejším fluórpolymérom, pretože má niekoľko vlastností, ktoré z neho robia ideálny materiál pre široké spektrum aplikácií.Je flexibilnejšia ako iné podobné rúry a odoláva takmer všetkým priemyselným chemikáliám
Teplotný rozsah je približne -330 °F až 500 °F, čo poskytuje najširší teplotný rozsah medzi fluórpolymérmi.Okrem toho má vynikajúce elektrické vlastnosti a nízku magnetickú permeabilitu.Ptfe hadičky sú najrozšírenejšie laboratórne hadičky a aplikácie, kde je nevyhnutná chemická odolnosť a čistota.PTFEmá veľmi nízky koeficient trenia a je jednou z najviac známych "sklzových" látok
Vlastnosti:
100% čistá PTFE živica
V porovnaní s FEP, PFA, HP PFA, UHP PFA, ETFE, ECTFE, najflexibilnejšími fluórpolymérovými rúrami
Chemicky inertný, odolný voči takmer všetkým priemyselným chemikáliám a rozpúšťadlám
Široký teplotný rozsah
Nízka penetrácia
Hladká nepriľnavá povrchová úprava
Najnižší koeficient trenia
Vynikajúci elektrický výkon
Nehorľavý
Netoxický
Aplikácie:
laboratórium
Chemický proces
Analytické a procesné zariadenia
Monitorovanie emisií
Nízka teplota
vysoká teplota
Elektrina
ozón
Štruktúra molekúl PTFE
Polytetrafluóretylén (PTFE) sa vyrába polymerizáciou mnohých molekúl tetrafluóretylénu
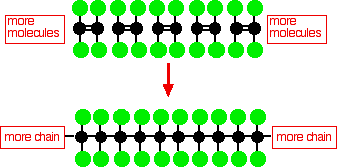
Tento jednoduchý PTFE diagram neukazuje trojrozmernú štruktúru molekuly.V jednoduchšom molekulárnom poly(etyléne) je uhlíková kostra molekuly spojená iba atómami vodíka a tento reťazec je veľmi flexibilný - rozhodne to nie je lineárna molekula
Avšak v polytetrafluóretyléne je atóm fluóru v skupine CF2 dostatočne veľký na to, aby interferoval s atómom fluóru na susednej skupine.Musíte si uvedomiť, že každý atóm fluóru má 3 páry osamelých elektrónov
Dôsledkom toho je potlačenie rotácie jednoduchej väzby uhlík-uhlík.Atómy fluóru majú tendenciu byť usporiadané tak, aby boli čo najďalej od susedných atómov fluóru.Rotácia má tendenciu zahŕňať kolízie osamelých párov medzi atómami fluóru na susedných atómoch uhlíka, čo spôsobuje, že rotácia je energeticky nepriaznivá
Odpudivá sila uzamkne molekulu do tvaru tyčinky a atómy fluóru sú usporiadané do veľmi jemnej špirály – atómy fluóru sú špirálovito usporiadané okolo uhlíkovej kostry.Tieto olovené pásiky budú stlačené dohromady ako dlhé tenké ceruzky v škatuľke
Toto tesné usporiadanie kontaktu má dôležitý vplyv na medzimolekulové sily, ako uvidíte
Medzimolekulové sily a teplota topenia PTFE
Teplota topenia polytetrafluóretylénu sa uvádza ako 327 °C.To je pre tento polymér dosť vysoké, takže medzi molekulami musia byť značné van der Waalsove sily
Prečo ľudia tvrdia, že van der Waalsove sily v PTFE sú slabé?
Van der Waalsova disperzná sila je spôsobená dočasnými kolísavými dipólmi generovanými pri pohybe elektrónov v molekule.Pretože molekula PTFE je veľká, očakávali by ste veľkú disperznú silu, pretože existuje veľa elektrónov, ktoré sa môžu pohybovať
Vo všeobecnosti platí, že čím väčšia molekula, tým väčšia disperzná sila
PTFE má však problém.Fluór je veľmi elektronegatívny.Má tendenciu viazať elektróny vo väzbe uhlík-fluór tak pevne, že sa elektróny nemôžu pohybovať, ako si myslíte.Opisujeme väzbu uhlík-fluór ako bez silnej polarizácie
Van der Waalsove sily zahŕňajú aj interakcie dipól-dipól.Ale v polytetrafluóretyléne (PTFE) je každá molekula obklopená vrstvou mierne záporne nabitých atómov fluóru.V tomto prípade je jedinou možnou interakciou medzi molekulami vzájomné odpudzovanie!
Takže disperzná sila je slabšia, ako si myslíte, a interakcia dipól-dipól spôsobí odpudzovanie.Niet divu, že ľudia hovoria, že van der Waalsova sila v PTFE je veľmi slabá.V skutočnosti nezískate odpudivú silu, pretože vplyv disperznej sily je väčší ako vplyv interakcie dipól-dipól, ale výsledný efekt je taký, že van der Waalsova sila bude mať tendenciu oslabovať.
Ale PTFE má veľmi vysoký bod topenia, takže sila, ktorá drží molekuly pohromade, musí byť veľmi silná
Ako môže mať PTFE vysoký bod topenia?
PTFE je veľmi kryštalický, v tomto zmysle ide o veľkú plochu, molekuly sú vo veľmi pravidelnom usporiadaní.Pamätajte, že molekuly PTFE možno považovať za predĺžené tyčinky.Tieto póly budú tesne spojené
To znamená, že hoci molekula ptfe nemôže produkovať skutočne veľké dočasné dipóly, dipóly sa dajú použiť veľmi efektívne
Sú teda van der Waalsove sily v PTFE slabé alebo silné?
Myslím, že pravdu môžete mať obaja!Ak sú polytetrafluóretylénové (PTFE) reťazce usporiadané tak, že medzi reťazami nie je príliš tesný kontakt, sila medzi nimi bude veľmi slabá a teplota topenia bude veľmi nízka.
Ale v reálnom svete sú molekuly v tesnom kontakte.Van der Waalsove sily nemusia byť také silné, ako môžu byť, ale štruktúra PTFE znamená, že pociťujú najväčší účinok, vytvárajúc celkovo silné medzimolekulové väzby a vysoké teploty topenia.
To je na rozdiel od iných síl, ako je sila interakcie dipól-dipól, ktorá sa zníži iba 23-krát alebo dvojnásobná vzdialenosť sa zníži 8-krát.
Preto tesné balenie molekúl v tvare tyčinky v PTFE maximalizuje účinnosť disperzie
Nepriľnavé vlastnosti
To je dôvod, prečo sa voda a olej nelepia na povrch PTFE a prečo môžete smažiť vajcia na panvici potiahnutej PTFE bez toho, aby sa prilepili na panvicu.
Musíte zvážiť, aké sily môžu fixovať iné molekuly na povrchuPTFE.Môže zahŕňať nejaký druh chemickej väzby, van der Waalsovej sily alebo vodíkovej väzby
Chemická väzba
Väzba uhlík-fluór je veľmi silná a nie je možné, aby akékoľvek iné molekuly dosiahli uhlíkový reťazec, aby došlo k akejkoľvek substitučnej reakcii.Je nemožné, aby došlo k chemickej väzbe
van der Waalsove sily
Videli sme, že van der Waalsova sila v PTFE nie je príliš silná a spôsobí, že PTFE bude mať len vysoký bod topenia, pretože molekuly sú tak blízko, že majú veľmi účinný kontakt.
Ale je to iné pre iné molekuly blízko povrchu PTFE.Relatívne malé molekuly (ako sú molekuly vody alebo molekuly oleja) budú mať len malý kontakt s povrchom a vytvorí sa len malé množstvo van der Waalsovej príťažlivosti.
Veľká molekula (napríklad proteín) nebude mať tvar tyčinky, takže medzi ňou a povrchom nie je dostatočne účinný kontakt na prekonanie nízkej polarizačnej tendencie PTFE.
V každom prípade je van der Waalsova sila medzi povrchom PTFE a okolitými vecami malá a neúčinná.
Vodíkové väzby
Molekuly PTFE na povrchu sú úplne obalené atómami fluóru.Tieto atómy fluóru sú veľmi elektronegatívne, takže všetky nesú určitý stupeň negatívneho náboja.Každý fluór má tiež 3 páry vyčnievajúcich osamelých elektrónov
Toto sú podmienky potrebné na vytvorenie vodíkových väzieb, ako je osamelý pár na fluóre a atóm vodíka vo vode.To sa však zjavne nestane, inak dôjde k silnej príťažlivosti medzi molekulami PTFE a molekulami vody a voda sa prilepí na PTFE.
Zhrnutie
Neexistuje žiadny účinný spôsob, ako by sa iné molekuly úspešne pripojili k povrchu PTFE, takže má nepriľnavý povrch
Nízke trenie
Koeficient trenia PTFE je veľmi nízky.To znamená, že ak máte povrch potiahnutý ptfe, ostatné veci sa vám na ňom ľahko šmýkajú.
Nižšie je rýchly súhrn toho, čo sa deje.Pochádza z dokumentu z roku 1992 s názvom „Trenie a opotrebovanie polytetrafluóretylénu“.
Na začiatku kĺzania sa povrch PTFE rozbije a hmota sa prenesie tam, kde sa kĺže.To znamená, že povrch PTFE sa opotrebuje.
Ako posúvanie pokračovalo, bloky sa rozvinuli do tenkých filmov.
Súčasne sa povrch PTFE vytiahne a vytvorí organizovanú vrstvu.
Oba povrchy, ktoré sú v kontakte, majú teraz dobre organizované molekuly PTFE, ktoré sa môžu po sebe kĺzať
Vyššie uvedené je zavedenie polytetrafluóretylénu, z polytetrafluóretylénu je možné vyrobiť rôzne produkty, špecializujeme sa na výrobu ptfe trubíc、výrobcovia ptfe hadíc, vitajte pri komunikácii s nami
Vyhľadávania súvisiace s hadicou ptfe:
Čas odoslania: máj-05-2021





