Polytetrafluorethyleen (polytetrafluorethyleen) is waarschijnlijk het meest gebruikte fluorpolymeer omdat het verschillende kenmerken heeft die het een ideaal materiaal maken voor een breed scala aan toepassingen.Het is flexibeler dan andere soortgelijke buizen en is bestand tegen bijna alle industriële chemicaliën
Het temperatuurbereik is ongeveer -330°F tot 500°F, wat het breedste temperatuurbereik onder fluorpolymeren oplevert.Bovendien heeft het uitstekende elektrische eigenschappen en een lage magnetische permeabiliteit.Ptfe-slangen zijn de meest gebruikte laboratoriumslangen en toepassingen waarbij chemische resistentie en zuiverheid essentieel zijn.PTFEheeft een zeer lage wrijvingscoëfficiënt en is een van de meest "slip" stoffen die we kennen
Functies:
100% pure PTFE-hars
Vergeleken met FEP, PFA, HP PFA, UHP PFA, ETFE, ECTFE, de meeste flexibele fluorpolymeerbuizen
Chemisch inert, bestand tegen vrijwel alle industriële chemicaliën en oplosmiddelen
Groot temperatuurbereik
Lage penetratie
Gladde anti-aanbaklaag
Laagste wrijvingscoëfficiënt
Uitstekende elektrische prestaties
Niet vlambaar
Niet giftig
Toepassingen:
laboratorium
Chemisch proces
Analyse- en procesapparatuur
Emissiemonitoring
Lage temperatuur
hoge temperatuur
Elektriciteit
ozon
De structuur van PTFE-moleculen
Polytetrafluorethyleen (PTFE) wordt gemaakt door de polymerisatie van veel tetrafluorethyleenmoleculen
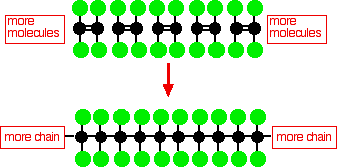
Dit eenvoudige PTFE-diagram toont niet de driedimensionale structuur van het molecuul.In het eenvoudigere moleculaire poly(ethyleen) is de koolstofruggengraat van het molecuul alleen verbonden door waterstofatomen, en deze keten is zeer flexibel: het is beslist geen lineair molecuul
In polytetrafluorethyleen is het fluoratoom in een CF2-groep echter groot genoeg om te interfereren met het fluoratoom van de aangrenzende groep.Je moet niet vergeten dat elk fluoratoom drie paar alleenstaande elektronen heeft die uitsteken
Het effect hiervan is dat de rotatie van de enkele koolstof-koolstofbinding wordt onderdrukt.De fluoratomen hebben de neiging zo te zijn gerangschikt dat ze zo ver mogelijk verwijderd zijn van de aangrenzende fluoratomen.Rotatie heeft de neiging om botsingen van één paar tussen fluoratomen op aangrenzende koolstofatomen met zich mee te brengen, wat de rotatie energetisch ongunstig maakt
De afstotende kracht zet het molecuul vast in de vorm van een staaf, en de fluoratomen zijn gerangschikt in een zeer zachte spiraal: de fluoratomen zijn gerangschikt in een spiraal rond de koolstofruggengraat.Deze loden strips worden samengedrukt als lange, dunne potloden in een doos
Dit nauwe contact heeft een belangrijke invloed op de intermoleculaire krachten, zoals je zult zien
Intermoleculaire krachten en het smeltpunt van PTFE
Het smeltpunt van polytetrafluorethyleen wordt vermeld als 327°C.Dit is vrij hoog voor dit polymeer, dus er moeten aanzienlijke Van der Waals-krachten tussen de moleculen zitten
Waarom beweren mensen dat de Van der Waals-krachten in PTFE zwak zijn?
De van der Waals-dispersiekracht wordt veroorzaakt door de tijdelijk fluctuerende dipolen die worden gegenereerd wanneer de elektronen in het molecuul rondbewegen.Omdat het PTFE-molecuul groot is, zou je een grote dispersiekracht verwachten omdat er veel elektronen zijn die kunnen bewegen
De algemene situatie is dat hoe groter het molecuul, hoe groter het dispersievermogen
PTFE heeft echter een probleem.Fluor is zeer elektronegatief.Het heeft de neiging de elektronen in de koolstof-fluorbinding stevig aan elkaar te binden, zo stevig dat de elektronen niet kunnen bewegen zoals je denkt.We beschrijven dat de koolstof-fluorbinding geen sterke polarisatie heeft
Van der Waals-krachten omvatten ook dipool-dipool-interacties.Maar in polytetrafluorethyleen (PTFE) is elk molecuul omgeven door een laag licht negatief geladen fluoratomen.In dit geval is de enige mogelijke interactie tussen moleculen wederzijdse afstoting!
De verspreidingskracht is dus zwakker dan je denkt, en de dipool-dipool-interactie zal afstoting veroorzaken.Geen wonder dat mensen zeggen dat de van der Waals-kracht in PTFE erg zwak is.Je krijgt niet echt de afstotende kracht, omdat de invloed van de verspreidingskracht groter is dan die van de dipool-dipool-interactie, maar het netto-effect is dat de van der Waals-kracht de neiging zal hebben om te verzwakken.
Maar PTFE heeft een zeer hoog smeltpunt, dus de kracht die de moleculen bij elkaar houdt moet erg sterk zijn
Hoe kan PTFE een hoog smeltpunt hebben?
PTFE is zeer kristallijn, in die zin is er een groot oppervlak, de moleculen zijn zeer regelmatig gerangschikt.Vergeet niet dat PTFE-moleculen kunnen worden gezien als langwerpige staven.Deze polen zullen dicht bij elkaar worden geclusterd
Dit betekent dat hoewel het ptfe-molecuul geen echt grote tijdelijke dipolen kan produceren, de dipolen zeer efficiënt kunnen worden gebruikt.
Zijn de van der Waals-krachten in PTFE dus zwak of sterk?
Ik denk dat jullie allebei gelijk kunnen hebben!Als de polytetrafluorethyleen (PTFE) kettingen zo zijn gerangschikt dat er geen te nauw contact tussen de kettingen is, zal de kracht ertussen erg zwak zijn en zal het smeltpunt erg laag zijn
Maar in de echte wereld staan moleculen in nauw contact.De Van der Waals-krachten zijn misschien niet zo krachtig als ze zijn, maar door de structuur van PTFE voelen ze het grootste effect, waardoor ze over het algemeen sterke intermoleculaire bindingen en hoge smeltpunten produceren.
Dit is in tegenstelling tot andere krachten, zoals de dipool-dipool-interactiekracht, die slechts 23 keer wordt verminderd, of tweemaal de afstand wordt verkleind met 8 keer
Daarom maximaliseert de strakke pakking van staafvormige moleculen in PTFE de effectiviteit van de dispersie
De antiaanbakeigenschappen
Dit is de reden waarom water en olie niet aan het oppervlak van PTFE blijven plakken, en waarom je eieren kunt bakken in een pan met PTFE-coating zonder dat ze aan de pan blijven plakken
Je moet overwegen welke krachten andere moleculen op het oppervlak kunnen fixerenPTFE.Het kan een soort chemische binding omvatten, van der Waals-kracht of waterstofbinding
Chemische binding
De koolstof-fluorbinding is erg sterk en het is onmogelijk dat andere moleculen de koolstofketen bereiken om een substitutiereactie te veroorzaken.Het is onmogelijk dat er een chemische binding ontstaat
van der Waals-troepen
We hebben gezien dat de van der Waals-kracht in PTFE niet erg sterk is en er alleen voor zorgt dat PTFE een hoog smeltpunt heeft, omdat de moleculen zo dichtbij zijn dat ze zeer effectief contact hebben.
Maar voor andere moleculen dicht bij het oppervlak van PTFE is het anders.Relatief kleine moleculen (zoals watermoleculen of oliemoleculen) zullen slechts een kleine hoeveelheid contact hebben met het oppervlak, en er zal slechts een kleine hoeveelheid van der Waals-aantrekkingskracht worden gegenereerd.
Een groot molecuul (zoals een eiwit) zal niet staafvormig zijn, dus er is niet voldoende effectief contact tussen het molecuul en het oppervlak om de lage polarisatieneiging van PTFE te overwinnen.
Hoe dan ook, de van der Waals-kracht tussen het oppervlak van de PTFE en de omringende dingen is klein en ineffectief
Waterstofbruggen
De PTFE-moleculen op het oppervlak zijn volledig omhuld door fluoratomen.Deze fluoratomen zijn zeer elektronegatief en hebben dus allemaal een zekere mate van negatieve lading.Elke fluor heeft ook 3 paar uitstekende alleenstaande elektronen
Dit zijn de omstandigheden die nodig zijn voor de vorming van waterstofbruggen, zoals het eenzame paar op fluor en het waterstofatoom in water.Maar dit zal uiteraard niet gebeuren, anders zal er een sterke aantrekkingskracht zijn tussen de PTFE-moleculen en de watermoleculen, en zal het water aan de PTFE blijven plakken.
Samenvatting
Er is geen effectieve manier waarop andere moleculen zich met succes aan het oppervlak van PTFE kunnen hechten, daarom heeft het een antiaanbaklaag
De lage wrijving
De wrijvingscoëfficiënt van PTFE is zeer laag.Dit betekent dat als je een oppervlak hebt dat is gecoat met ptfe, er gemakkelijk andere dingen op kunnen glijden.
Hieronder vindt u een korte samenvatting van wat er gebeurt.Dit komt uit een artikel uit 1992 getiteld "Wrijving en slijtage van polytetrafluorethyleen".
Aan het begin van het glijden breekt het PTFE-oppervlak en wordt de massa overgebracht naar de plek waar deze glijdt.Dit betekent dat het PTFE-oppervlak zal slijten.
Terwijl het glijden voortduurde, ontvouwden de blokken zich tot dunne films.
Tegelijkertijd wordt het oppervlak van de PTFE eruit getrokken om een georganiseerde laag te vormen.
Beide oppervlakken die met elkaar in contact komen, hebben nu goed georganiseerde PTFE-moleculen die over elkaar kunnen glijden
Het bovenstaande is de introductie van polytetrafluorethyleen, polytetrafluorethyleen kan in een verscheidenheid aan producten worden verwerkt, wij zijn gespecialiseerd in het maken van ptfe-buizen.fabrikanten van ptfe-slangen, welkom om met ons te communiceren
Zoekopdrachten gerelateerd aan ptfe slang:
Posttijd: 05 mei 2021





