Polytetrafluorethylen (Polytetrafluorethylen) ist wahrscheinlich das am weitesten verbreitete Fluorpolymer, da es mehrere Eigenschaften aufweist, die es zu einem idealen Material für eine Vielzahl von Anwendungen machen.Es ist flexibler als andere ähnliche Rohre und beständig gegen nahezu alle Industriechemikalien
Der Temperaturbereich beträgt etwa -330 °F bis 500 °F und bietet damit den größten Temperaturbereich unter Fluorpolymeren.Darüber hinaus verfügt es über hervorragende elektrische Eigenschaften und eine geringe magnetische Permeabilität.PTFE-Schläuche sind die am häufigsten verwendeten Laborschläuche und Anwendungen, bei denen chemische Beständigkeit und Reinheit von entscheidender Bedeutung sind.PTFEhat einen sehr niedrigen Reibungskoeffizienten und ist einer der „gleitfähigsten“ Stoffe, die es gibt
Merkmale:
100 % reines PTFE-Harz
Im Vergleich zu FEP, PFA, HP PFA, UHP PFA, ETFE, ECTFE, den meisten flexiblen Fluorpolymerrohren
Chemisch inert, beständig gegen fast alle Industriechemikalien und Lösungsmittel
Großer Temperaturbereich
Geringe Penetration
Glatte, antihaftbeschichtete Oberfläche
Niedrigster Reibungskoeffizient
Hervorragende elektrische Leistung
Nicht brennbar
Ungiftig
Anwendungen:
Labor
Chemischer Prozess
Analyse- und Prozessausrüstung
Emissionsüberwachung
Niedrige Temperatur
hohe Temperatur
Elektrizität
Ozon
Die Struktur von PTFE-Molekülen
Polytetrafluorethylen (PTFE) wird durch Polymerisation vieler Tetrafluorethylenmoleküle hergestellt
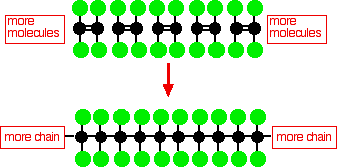
Dieses einfache PTFE-Diagramm zeigt nicht die dreidimensionale Struktur des Moleküls.Im einfacheren molekularen Polyethylen ist das Kohlenstoffgerüst des Moleküls nur durch Wasserstoffatome verbunden, und diese Kette ist sehr flexibel – es handelt sich definitiv nicht um ein lineares Molekül
Allerdings ist in Polytetrafluorethylen das Fluoratom in einer CF2-Gruppe groß genug, um mit dem Fluoratom in der benachbarten Gruppe zu interferieren.Sie müssen bedenken, dass jedes Fluoratom drei Paare freistehender Elektronen aufweist
Dadurch wird die Rotation der Kohlenstoff-Kohlenstoff-Einfachbindung unterdrückt.Die Fluoratome werden tendenziell so angeordnet, dass sie möglichst weit von den benachbarten Fluoratomen entfernt sind.Bei der Rotation kommt es tendenziell zu Kollisionen einzelner Elektronenpaare zwischen Fluoratomen und benachbarten Kohlenstoffatomen, was die Rotation energetisch ungünstig macht
Die abstoßende Kraft fixiert das Molekül in einer Stabform und die Fluoratome sind in einer sehr sanften Spirale angeordnet – die Fluoratome sind spiralförmig um das Kohlenstoffrückgrat angeordnet.Diese Minenstreifen werden wie lange, dünne Bleistifte in einer Schachtel zusammengedrückt
Wie Sie sehen werden, hat diese enge Kontaktanordnung einen wichtigen Einfluss auf die zwischenmolekularen Kräfte
Intermolekulare Kräfte und der Schmelzpunkt von PTFE
Der Schmelzpunkt von Polytetrafluorethylen wird mit 327°C angegeben.Dieser ist für dieses Polymer recht hoch, sodass zwischen den Molekülen erhebliche Van-der-Waals-Kräfte herrschen müssen
Warum wird behauptet, die Van-der-Waals-Kräfte in PTFE seien schwach?
Die Van-der-Waals-Dispersionskraft wird durch die vorübergehend schwankenden Dipole verursacht, die entstehen, wenn sich die Elektronen im Molekül bewegen.Da das PTFE-Molekül groß ist, würde man eine große Dispersionskraft erwarten, da es viele Elektronen gibt, die sich bewegen können
Generell gilt, dass die Dispersionskraft umso größer ist, je größer das Molekül ist
Allerdings hat PTFE ein Problem.Fluor ist sehr elektronegativ.Es neigt dazu, die Elektronen in der Kohlenstoff-Fluor-Bindung fest aneinander zu binden, so fest, dass sich die Elektronen nicht so bewegen können, wie man denkt.Wir beschreiben die Kohlenstoff-Fluor-Bindung als nicht stark polarisiert
Van-der-Waals-Kräfte umfassen auch Dipol-Dipol-Wechselwirkungen.Bei Polytetrafluorethylen (PTFE) ist jedoch jedes Molekül von einer Schicht leicht negativ geladener Fluoratome umgeben.In diesem Fall ist die einzig mögliche Wechselwirkung zwischen Molekülen die gegenseitige Abstoßung!
Die Dispersionskraft ist also schwächer als Sie denken, und die Dipol-Dipol-Wechselwirkung führt zu Abstoßung.Kein Wunder, dass die Leute sagen, dass die Van-der-Waals-Kraft in PTFE sehr schwach ist.Die abstoßende Kraft wird nicht tatsächlich auftreten, da der Einfluss der Dispersionskraft größer ist als der der Dipol-Dipol-Wechselwirkung, aber der Nettoeffekt besteht darin, dass die Van-der-Waals-Kraft tendenziell schwächer wird
Da PTFE jedoch einen sehr hohen Schmelzpunkt hat, muss die Kraft, die die Moleküle zusammenhält, sehr stark sein
Wie kann PTFE einen hohen Schmelzpunkt haben?
PTFE ist sehr kristallin, in diesem Sinne gibt es eine große Fläche, die Moleküle sind in einer sehr regelmäßigen Anordnung.Denken Sie daran, dass man sich PTFE-Moleküle als längliche Stäbe vorstellen kann.Diese Pole werden eng beieinander liegen
Das bedeutet, dass das PTFE-Molekül zwar keine wirklich großen temporären Dipole erzeugen kann, die Dipole jedoch sehr effizient genutzt werden können
Sind die Van-der-Waals-Kräfte in PTFE also schwach oder stark?
Ich denke, Sie können beide Recht haben!Wenn die Ketten aus Polytetrafluorethylen (PTFE) so angeordnet sind, dass kein zu enger Kontakt zwischen den Ketten entsteht, ist die Kraft zwischen ihnen sehr schwach und der Schmelzpunkt sehr niedrig
Aber in der realen Welt stehen Moleküle in engem Kontakt.Van-der-Waals-Kräfte sind vielleicht nicht so stark, wie sie vielleicht sind, aber aufgrund der Struktur von PTFE spüren sie die größte Wirkung und erzeugen insgesamt starke intermolekulare Bindungen und hohe Schmelzpunkte
Dies steht im Gegensatz zu anderen Kräften, wie etwa der Dipol-Dipol-Wechselwirkungskraft, die nur um das 23-fache reduziert wird, oder der doppelten Entfernung, die um das 8-fache reduziert wird
Daher maximiert die dichte Packung der stäbchenförmigen Moleküle in PTFE die Wirksamkeit der Dispersion
Die Antihafteigenschaften
Aus diesem Grund haften Wasser und Öl nicht an der Oberfläche von PTFE und Sie können Eier in einer PTFE-beschichteten Pfanne braten, ohne dass sie an der Pfanne kleben bleiben
Sie müssen überlegen, welche Kräfte andere Moleküle auf der Oberfläche fixieren könntenPTFE.Es kann sich um eine Art chemische Bindung, eine Van-der-Waals-Kraft oder eine Wasserstoffbindung handeln
Chemische Verbindung
Die Kohlenstoff-Fluor-Bindung ist sehr stark und es ist für andere Moleküle unmöglich, die Kohlenstoffkette zu erreichen und eine Substitutionsreaktion auszulösen.Eine chemische Bindung ist ausgeschlossen
Van-der-Waals-Kräfte
Wir haben gesehen, dass die Van-der-Waals-Kraft in PTFE nicht sehr stark ist und nur dazu führt, dass PTFE einen hohen Schmelzpunkt hat, weil die Moleküle so nah beieinander sind, dass sie einen sehr effektiven Kontakt haben.
Anders verhält es sich jedoch mit anderen Molekülen nahe der Oberfläche von PTFE.Relativ kleine Moleküle (wie Wassermoleküle oder Ölmoleküle) haben nur einen geringen Kontakt mit der Oberfläche und es wird nur eine geringe Van-der-Waals-Anziehung erzeugt.
Ein großes Molekül (z. B. ein Protein) ist nicht stabförmig, sodass zwischen ihm und der Oberfläche kein ausreichend wirksamer Kontakt besteht, um die geringe Polarisationsneigung von PTFE zu überwinden.
In jedem Fall ist die Van-der-Waals-Kraft zwischen der Oberfläche des PTFE und den umgebenden Dingen gering und unwirksam
Wasserstoffbrücken
Die PTFE-Moleküle auf der Oberfläche sind vollständig von Fluoratomen umhüllt.Diese Fluoratome sind sehr elektronegativ, daher tragen sie alle einen gewissen Grad an negativer Ladung.Jedes Fluor verfügt außerdem über 3 Paare hervorstehender einzelner Elektronen
Dies sind die Bedingungen, die für die Bildung von Wasserstoffbrückenbindungen erforderlich sind, beispielsweise des freien Elektronenpaars am Fluor und des Wasserstoffatoms in Wasser.Aber das wird natürlich nicht passieren, da sonst eine starke Anziehung zwischen den PTFE-Molekülen und den Wassermolekülen entsteht und das Wasser am PTFE haften bleibt
Zusammenfassung
Für andere Moleküle gibt es keine wirksame Möglichkeit, sich erfolgreich an die Oberfläche von PTFE zu binden, daher verfügt es über eine antihaftbeschichtete Oberfläche
Die geringe Reibung
Der Reibungskoeffizient von PTFE ist sehr niedrig.Das heißt, wenn Sie eine mit PTFE beschichtete Oberfläche haben, können andere Dinge leicht darauf verrutschen.
Nachfolgend finden Sie eine kurze Zusammenfassung dessen, was passiert.Dies geht aus einer Arbeit aus dem Jahr 1992 mit dem Titel „Friction and Wear of Polytetrafluorethylen“ hervor.
Zu Beginn des Gleitens bricht die PTFE-Oberfläche und die Masse wird dorthin übertragen, wo sie gleitet.Dies bedeutet, dass die PTFE-Oberfläche verschleißt.
Während das Gleiten weiterging, entfalteten sich die Blöcke zu dünnen Filmen.
Gleichzeitig wird die Oberfläche des PTFE herausgezogen, um eine organisierte Schicht zu bilden.
Beide Kontaktflächen verfügen nun über gut organisierte PTFE-Moleküle, die aufeinander gleiten können
Das Obige ist die Einführung von Polytetrafluorethylen. Polytetrafluorethylen kann zu einer Vielzahl von Produkten verarbeitet werden. Wir sind auf die Herstellung von PTFE-Röhren spezialisiert.Hersteller von PTFE-Schläuchen, willkommen, mit uns zu kommunizieren
Suchanfragen zum Thema PTFE-Schlauch:
Zeitpunkt der Veröffentlichung: 05.05.2021





